金属离子团簇材料广泛存在于人体骨骼、血液中,凭借其可控的生物降解特性及优异的生物相容性、生物活性,已在骨缺损修复、口腔硬组织再生等领域展现出重大的临床治疗潜力。然而,该类材料固有的热力学亚稳态特征、自发晶化趋势、以及尚不明确的生物学作用机制,严重制约了其临床广泛应用。
近期,中国科学院金属研究所仿生医用材料课题组张兴研究员团队在前期提出聚丙烯酸分子调控金属磷酸盐团簇热稳定性(Bioactive Materials 6 (2021) 2303-2314)及锌掺杂非晶磷酸钙(ACZP)团簇的骨免疫调节再生机制(Journal of Materials Science & Technology 226 (2025) 320-333;Bioactive Materials 52 (2025) 829-844)研究基础上,进一步深入探究金属离子团簇在大尺寸骨缺损修复中的生物功能,以解决该领域长期面临的支架材料难以兼顾足够力学支撑与优异生物活性的核心瓶颈难题。
该研究受螳螂虾附肢中“马鞍”外层高矿化、内层富有机相的梯度层状结构启发,以ACZP为核心组装活性单元,通过多级组装策略构建一种集“结构仿生”、“成分仿生”和“功能仿生”于一体的ACZP/几丁质(ACZP/CT)骨修复支架。该支架形成了高矿化致密外层结合有机质层状纤维内层的梯度结构;其中尺寸为1-2 nm的ACZP纳米团簇进一步组装成约250 nm的团聚体。经60℃热压后支架成功保持了非晶相结构;热重分析显示,支架外层矿物含量约为62.02%,内层约为21.39%,体现出明显的梯度矿化特征。在力学性能方面,该仿生支架弯曲强度约为160.09 MPa,断裂韧性最高可达10.08 MPa·m1/2,显示出优异的承载能力,这种优异韧性源于梯度层间复杂裂纹扩展、纤维撕裂、矿物-纤维脱黏以及层间滑移等多重耗能机制的协同作用。在生物学方面,ACZP/CT支架能够通过持续释放的Ca²⁺和Zn²⁺协同激活PI3K-Akt、MAPK和HIF-1等关键信号通路,从而显著促进成骨细胞分化、内皮细胞血管化及成骨耦合。此外,动物实验步证实,该支架在大鼠颅骨缺损模型中表现出优异修复能力,植入6个月后新生骨体积分数达到68.39%,显示出良好的骨再生效果。由此,这种基于ACZP金属离子团簇作为组装单元构建的“结构-成分-功能”仿生骨修复支架,兼具高强度、高韧性与高生物活性,为大尺寸骨缺损修复提供了极具临床转化潜力的崭新策略。
相关结果以“Mantis shrimp saddle-mimetic amorphous calcium (zinc) phosphate/chitin scaffolds with superior mechanical properties and bioactivity for bone regeneration”为题发表于Bioactive Materials 58 (2026) 738–754。
金属所博士生赵紫濠与解放军总医院骨科医学部博士后高建朋为共同第一作者,解放军总医院骨科医学部李明教授与张兴研究员为共同通讯作者。该研究工作得到了国家自然科学基金、国家重点研发计划等项目资助。
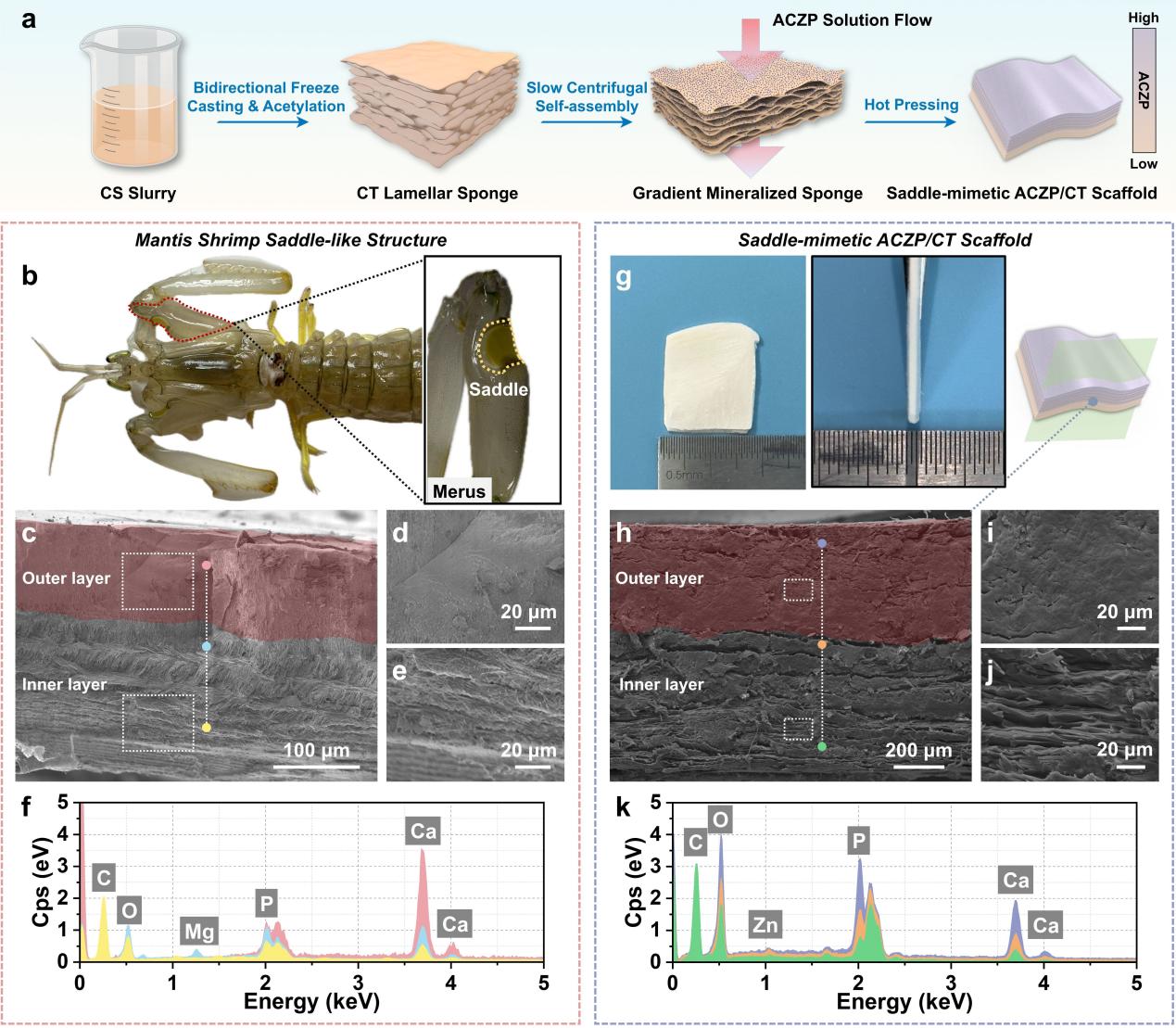
图1 天然螳螂虾“马鞍”结构与仿生ACZP/CT支架制备
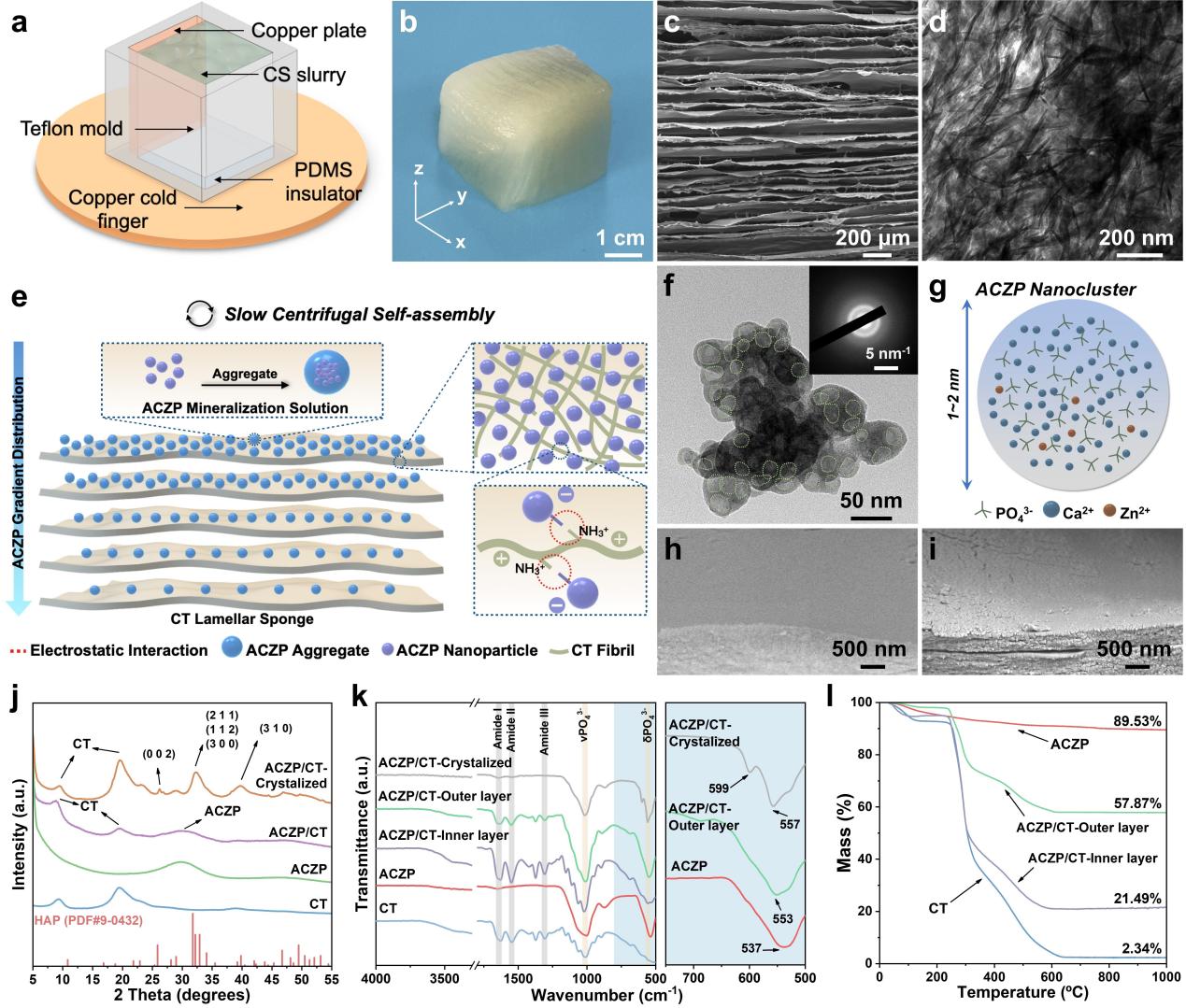
图2 仿生ACZP/CT支架制备过程及相组成、微观结构表征
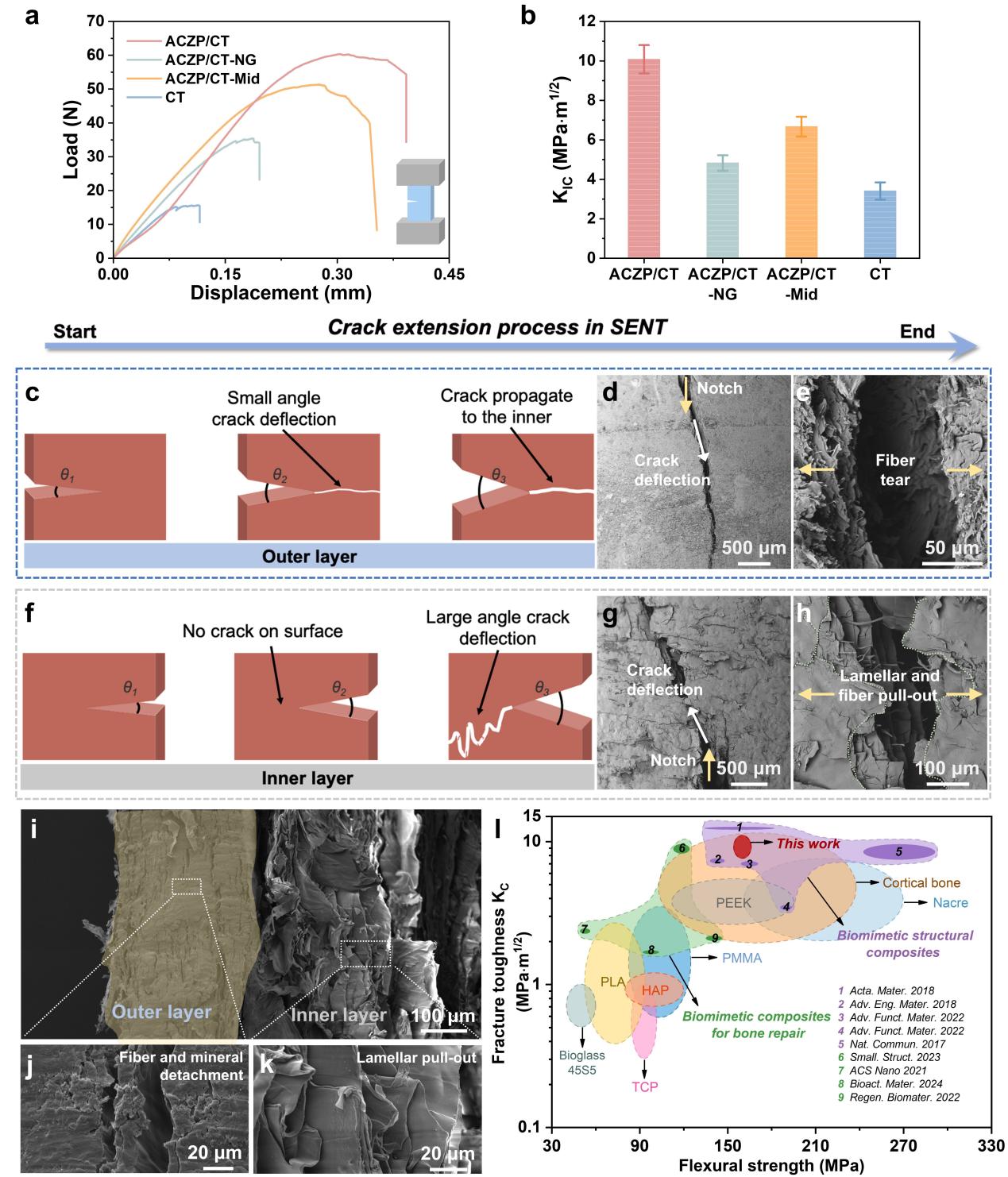
图3 仿生ACZP/CT支架裂纹扩展路径与增韧机制分析
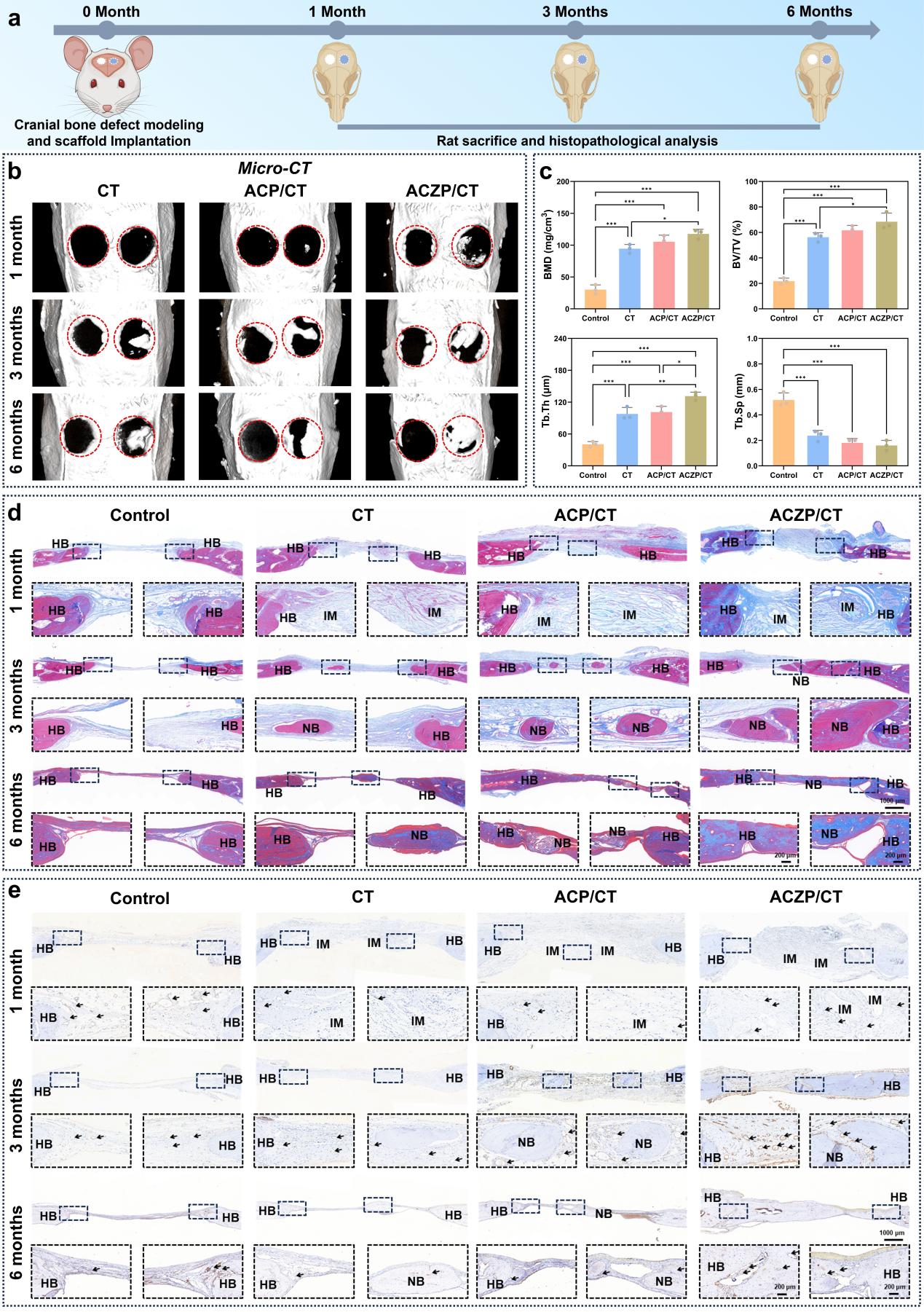
图4 仿生ACZP/CT支架在大鼠颅骨缺损模型中的骨修复效果评价
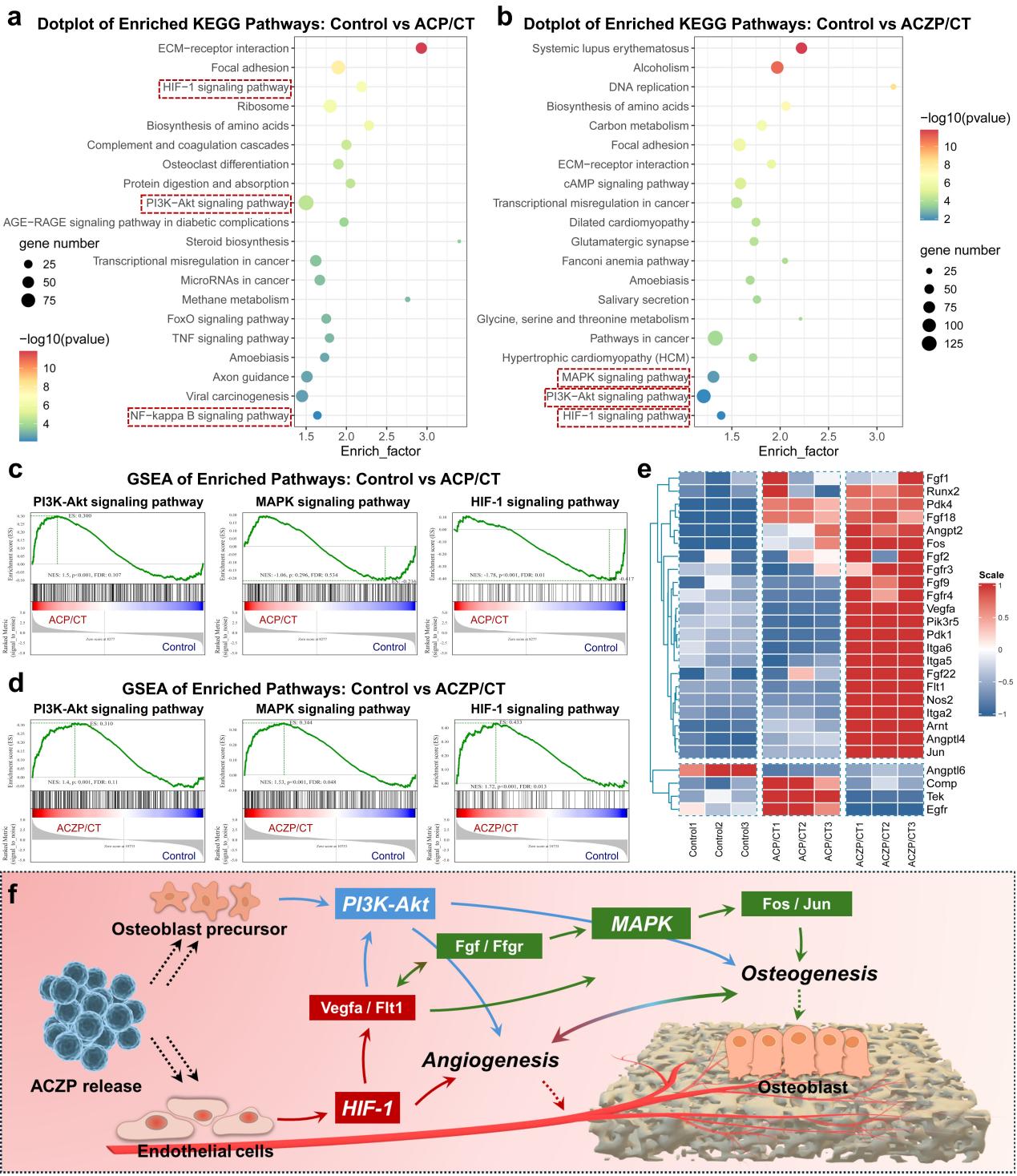
图5 仿生ACZP/CT支架血管生成-成骨耦合机制分析



